微生物感染导致阿尔茨海默病?
一个认为感染导致阿尔茨海默病的大胆猜想,试图解释为何数十年来对这一疾病的治疗效果甚微。

一个认为感染导致阿尔茨海默病的大胆猜想,试图解释为何数十年来对这一疾病的治疗效果甚微。
每周五下午,波士顿麻省总医院的神经科医生罗伯特·莫尔(Robert Moir)都会沉迷于他的“玩耍时间”。但他既不是去健身房,也不是去酒吧,而是拿着一瓶啤酒在电脑前坐下,浏览PubMed(美国国家医学图书馆的生命科学期刊研究摘要数据库)。莫尔在PubMed上四处寻找隐藏的杰作:那些为他提供新视角的研究,或者引导他走向新方向的研究。2007年5月11日,喝着啤酒的莫尔,偶然发现了一组即将改变他职业生涯的研究报告。
莫尔研究阿尔茨海默病,更具体地说,他研究的是β-淀粉样蛋白,这种蛋白在阿尔茨海默病患者的大脑中聚集成大而粗糙的斑块。根据目前流行的β-淀粉样蛋白假说,大脑中β-淀粉样蛋白的积累会直接导致阿尔茨海默病——它激发了神经元内tau蛋白(阿尔茨海默病的主要标记)的缠结和累积,导致细胞死亡,最终致人痴呆。大多数科学家认为,β-淀粉样蛋白斑块没有什么好处,只会造成毁灭性的生物事故。
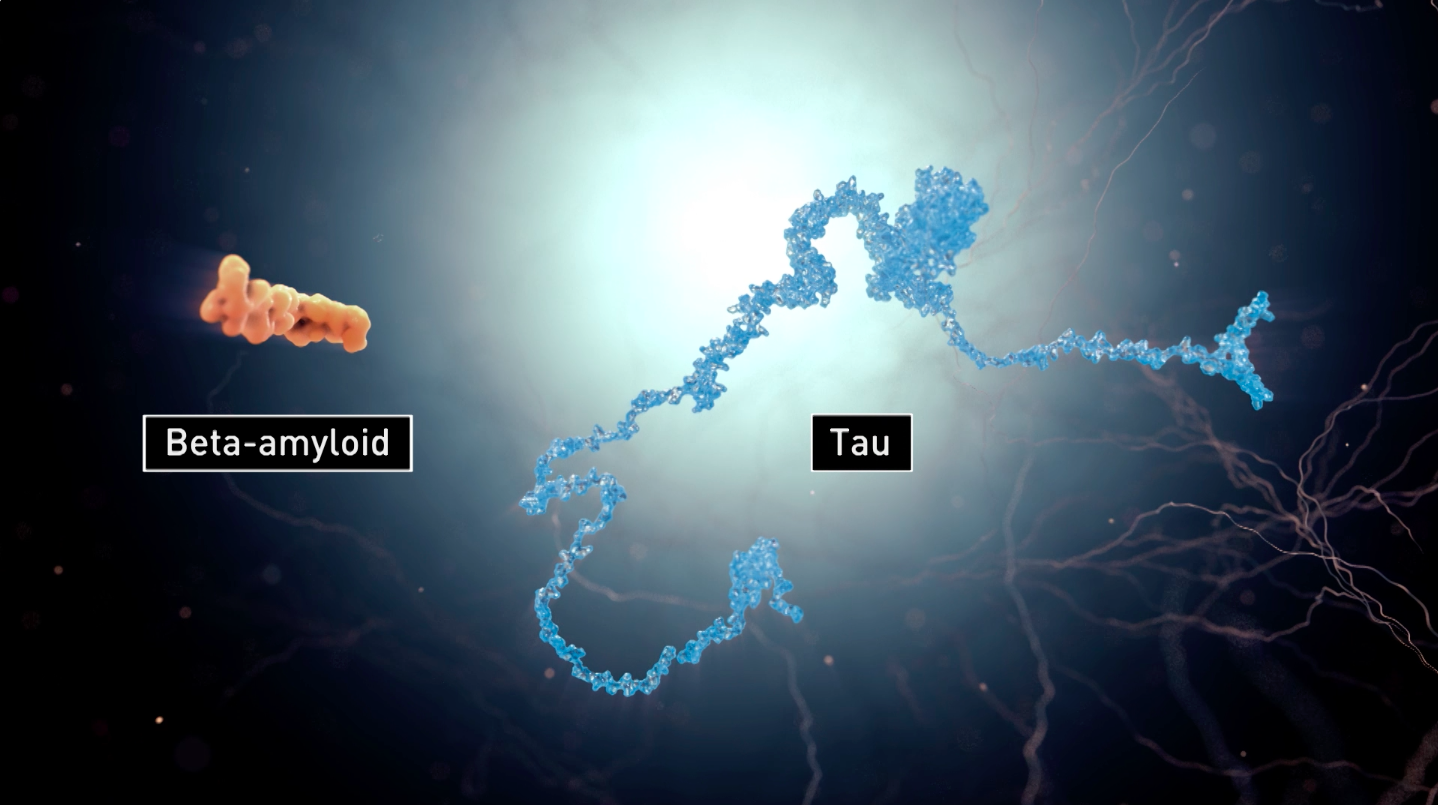
在那个决定性的一天,莫尔发现了挑战这一观点的研究。他偶然发现一系列关于LL-37的论文,LL-37是一种抗菌肽,在机体抵抗入侵病原体的快速防御中起着至关重要的作用。莫尔回忆道:“我立即被LL-37与β-淀粉样蛋白的基因序列不同,但作用非常相似震惊到了。” 他开始编纂一份长达四页,有关这两种蛋白共有分子特征的清单。莫尔的发现指向了一个激进的想法:β-淀粉样蛋白,就像关键的免疫肽一样,是防御大脑走向阿尔茨海默病的一部分。
莫尔和他的同事此后发表了一系列研究报告,最新一篇发表在2016年3月刊的《科学-转化医学》(Science Translational Medicine)上,表明β-淀粉样蛋白是大脑中一种有效的抗病原体分子。他们的报告指出,小鼠的大脑在感染β-淀粉样蛋白后的数小时内积累淀粉样斑块,这些斑块有助于它们活得更久。他们还在实验室直接观察到了杀死病原体的β-淀粉样蛋白。
而他们的发现也为处于争议中心的“病原体假说”添砖加瓦,此假说几十年来一直吸引着一小批研究人员。病原体假说认为微生物在阿尔茨海默病中起着重要作用,而β-淀粉样斑块实际上如同机体对抗微生物的士兵,虽然这场战斗最终陷入混乱,导致大量脑细胞死亡。2015年,澳大利亚的研究人员在一篇对25项已发表的研究进行的元分析中指出,受某些类型细菌感染的人患阿尔茨海默病的可能性高出10倍。同时,2016年3月,33名国际研究人员在《阿尔茨海默病杂志》(Journal of Alzheimer’s Disease)上共同签署了一篇社论,呼吁其他人认真考虑阿尔茨海默病的根源来自细菌感染。
虽然学界仍然认为病原体假说牵强附会——这的确是一种可能,然而支持这个假说的相关实验样本太小。这种说法可能没错,不过研究人员试图突破主流观点时面临的障碍,以及说服反对者所需的举证责任也值得深思。大脑研究有着巨大的技术局限:科学家们不能撬开活人的头颅做实验,而在那里寻找微生物就更难了,因为大多数病原体隐藏在细胞内部,有时还会嵌入基因组中。即使科学家们找到可靠方法来研究病原体假设,他们也不一定能获得资金支持;就算获得了资助做实验,他们也很难把发现公开发表。例如,莫尔那篇发表于2016年的论文被接收之前,连续六次未审查便被拒绝了。“这太残忍了,”莫尔回忆道。
更为复杂的问题在于,如果细菌感染和阿尔茨海默病之间确实存在关联,那么这种关联几乎肯定会是复杂的,由多因素构成。微生物可能只是开始,往后还有涉及基因、炎症以及环境影响的一连串因素,这使得这一观点更难得到验证,也更容易产生误解。
虽然病原体假说是否有价值仍然存疑,但至关重要的是,要把这一理论的弱点从科学的局限性和那些急于否定它的人的偏见中分离出来。

····
感染可以侵入大脑并影响认知的观念并不新鲜,而且已被研究证实。1911年,阿洛伊斯·阿尔茨海默(Alois Alzheimer)发现梅毒性痴呆患者和阿尔茨海默病患者的大脑有相似之处。如果梅毒在体内感染超过10年,一种螺旋形细菌会侵入并损害大脑,引发淀粉样斑块的形成,诱发痴呆。单纯疱疹病毒性脑炎,是一种罕见的由单纯疱疹病毒-1型(HSV-1,引起唇疱疹的病毒)引发的并发症,可以导致脑损伤;蜱传莱姆病可引起记忆丧失和脑炎症;随着时间的推移,人类免疫缺陷病毒(HIV)也会导致痴呆;还有寨卡病毒,这种由蚊子传播的病毒可以侵入发育中的大脑,限制它的大小和发育。
科学家们研究得越多,就越发现大脑——这个历史上曾被认为是受血脑屏障保护的无菌器官,经常被微生物渗透。微生物以多种方式进入大脑:单纯疱疹病毒-1型会感染眼睛的角膜,然后侵入三叉神经中的细胞,经由三叉神经传到大脑。艾滋病病毒采用类似“特洛伊木马”似的进攻——先在血液中感染免疫细胞,然后进入大脑。弓形虫已经感染了近四分之一的美国人口,它通过内皮细胞潜入大脑。一些口腔细菌——那些与蛀牙和牙龈炎有关的细菌——则通过嗅球潜入大脑,嗅球是大脑附近一个神经高度发达的区域。
然而这些研究并不能证明细菌感染会引发阿尔茨海默病,它们只是暗示两者相互关联。
病理学家艾伦·麦克唐纳(Alan MacDonald)首次记录了阿尔茨海默病患者大脑中的微生物。他的祖父患有阿尔茨海默病,祖父的去世激发了他研究阿尔茨海默病的兴趣。1986年,当时在长岛南安普敦医院的麦克唐纳在给《美国医学协会杂志》(Journal of the American Medical Association)编辑的一封信中描述,他在两名阿尔茨海默病患者的大脑中发现导致莱姆病的细菌。后来他从其他几个阿尔茨海默病患者的大脑中培养出了莱姆病活菌。7年后的1993年,瑞士洛桑大学的神经病学家和神经病理学家朱迪丝·米库洛丝(Judith Miklossy)从14名阿尔茨海默病患者的大脑中分离出了莱姆病细菌,但在13名非阿尔茨海默病患者的大脑中未找到同样的细菌。
肺炎衣原体能引起肺炎,是另一种与阿尔茨海默病有关的病原体。大多数感染这种细菌的人会发展成慢性潜伏感染,而这些微生物通常会在细胞内潜伏数年。尽管他们的发现无法被研究重复,费城骨科医学院老年慢性疾病中心主任布赖恩·巴林(Brian Balin)和他的同事在19个阿尔茨海默病患者的17个中发现了肺炎衣原体基因,但在19个非患病大脑中只发现了1个携带此基因。与此同时,英国曼彻斯特大学的神经生物学家露丝·伊扎克(Ruth Itzhaki)和她的同事们已经研究单纯疱疹病毒-1型(HSV-1)与阿尔茨海默病之间的关系超过20年。研究表明,如果一个人的大脑中含有单纯疱疹病毒-1型(HSV-1)和载脂蛋白E4(APOE4)基因变体,那么他患阿尔茨海默病的风险就会高出12倍,此外,这种基因变体还会增强病毒在大脑中的感染能力。研究人员还发现,阿尔茨海默病患者大脑的神经元内部潜伏着真菌。
这些研究并不能证明感染会导致阿尔茨海默病,它们只是暗示两者相互关联。例如,阿尔茨海默病患者可能特别容易受到感染,这样因果关系就不成立了。然而,一些研究的确表明感染在前。莫尔的研究表明,只有在受到沙门氏菌感染后,β-淀粉样斑块才会在小鼠大脑中积聚;2014年巴林和他的同事用肺炎衣原体感染小鼠时,也得到了相同的结果。其他研究报告称,单纯疱疹病毒-1型会周期性地从潜伏状态出现,而血液中含有最近重新激活的这种病毒抗体的人,相比没有这种抗体的人在许多年后患阿尔茨海默病的可能性高出一倍。
····
病原体假说的大多数支持者并不认为仅仅感染就可导致阿尔茨海默病,也不认为阿尔茨海默病可以像感冒一样“感染”。相反,他们认为感染(可能是多种不同类型)会引发一连串事件,随着时间的推移,最终导致疾病。哥伦比亚大学感染和免疫转化研究中心的主任麦迪·霍尼格(Mady Hornig)说:“这些微生物本身可能不是具体病因,而是疾病退化过程的促成因素。”
退化过程也许是这样开始的:大脑受到损伤或感染,再由积累β-淀粉样蛋白斑块来修复问题。β-淀粉样蛋白可能具有保护作用的想法,最早由澳大利亚神经病学家斯蒂芬·罗宾逊(Stephen Robinso)和格兰达·毕晓普(Glenda Bishop)在2002年的一篇论文中提出。他们指出,在严重的脑损伤后,淀粉样斑块会累积。(其实在过去的4亿年中,β-淀粉样蛋白也没有多大变化,并且在多数脊椎动物中发现,这进一步支持了β-淀粉样蛋白具有重要作用的观点。)莫尔于2016年发表在《科学-转化医学》杂志上的研究表明,实际上,β-淀粉样蛋白通过将自身附着在病原体上,然后形成包裹和截留微生物的原纤维,从而保护大脑免受微生物的侵害。莫尔和他的同事在注射沙门氏菌数小时后的小鼠大脑中,发现了广泛分布的β-淀粉样斑块。
血脑屏障随年龄增长而变得更易渗透,也许在年岁已高时,微生物将更容易穿透它。
感染之后,随着β-淀粉样斑块积累足够多时,它们也会成为问题。莫尔解释说:“病原体死后很久,淀粉样斑块仍然存在,并导致一系列炎症。”正如他的同事在2014年发表于《自然》的一篇论文中所指出的那样,淀粉样斑块会导致tau缠结,而tau缠结将直接杀死神经元。同时,斑块也提醒小胶质细胞这个大脑的免疫监督者,有什么东西出了问题;然后小胶质细胞则会进入进攻模式,释放免疫化学物质和活性氧物质来杀死微生物,但它们也会损伤神经元。麻省总医院遗传和衰老研究部主任鲁道夫·坦齐(Rudolph Tanzi)解释说:“正是这种友好的提醒可能会导致更多的神经元死亡。”
此外,一些研究人员认为,大脑以外的感染也有影响阿尔茨海默病的风险。英国南安普敦大学的神经病理学专家V·休·派瑞(V Hugh Perry)说:“大脑中有一些回路,会被系统性感染激发,系统性感染不是通过感染进入大脑,而是通过多种不同的途径与大脑进行沟通。”一些微生物可能会触发大脑外免疫分子的激活,然后进入大脑,对其产生影响;另一些可能会导致身体产生自我攻击抗体,损害脑细胞。2015年发表在《欧洲神经病学杂志》(European Journal of Neurology)上的一项研究发现,具有抵抗常见系统性感染抗体的人患阿尔茨海默病的风险的确更高。
但即使阿尔茨海默病最初是由某种感染引发的,疾病风险无疑也由其他因素决定。首先,年龄是很重要的一个因素:大多数人在65岁以后才会发病。研究表明,随着年龄的增长,血脑屏障变得更易渗透,也许在年岁已高时,微生物将更容易穿透它。随着年龄的增长,小胶质细胞也变得越来越活跃,使炎症反应变得更加强烈和危险。其次,基因也起着至关重要的作用;阿尔茨海默病的一些早期发病形式仅由罕见的基因突变引起,而其他基因变异可使大脑更容易受到感染的影响,使感染的炎症反应更具破坏性,或者如载脂蛋白E4(APOE4)一样,影响病原体进入大脑的能力。即使感染确实在阿尔茨海默病中起着因果作用,一个人的患病风险也会受到其他因素影响,这使得整个过程更破朔迷离。
····
对病原体假说的研究已有二十余年,但在阿尔茨海默病学界却鲜有讨论。2016年,在《神经化学杂志》(Journal of Neurochemistry)60周年特刊上的一篇论文中,研究人员讨论了关于阿尔茨海默病病因的六个假说(这些假说与目前流行的淀粉样级联模型相竞争),但病原体假说不包括在其中。当然,病原体假说只有有限的间接证据支持,而淀粉样蛋白级联假说却有一些令人信服的直接证据。
淀粉样蛋白级联假说诞生于1992年,当时的研究者发现β-淀粉样蛋白前体(以下简称APP)的突变导致早发性阿尔茨海默病。患有唐氏综合征的人有三个制造APP的基因拷贝,他们特别容易患早发性疾病。这些发现表明,当身体的基因指令告诉它制造额外的β-淀粉样蛋白时,阿尔茨海默病随之而来。但大多数阿尔茨海默病患者并没有这种遗传性的早发性疾病。大多数人患有所谓的“散发性”阿尔茨海默症,这种病通常发生在晚年,与早发性完全不同。
根据淀粉样蛋白级联假说,大脑中的β-淀粉样蛋白斑块的积累是散发性阿尔茨海默病的主要原因。根据这个定义,大脑中满是斑块的人应该患有阿尔茨海默症。但结果往往不是这样:验尸结果标明,1/4到1/3的非阿尔茨海默病患者的大脑中也充满淀粉样斑块。
有趣的是,小胶质细胞是大脑中的免疫细胞,它的行为可以在一定程度上区分这些所谓的“弹性”大脑和患有阿尔茨海默病的大脑。在2013年的一项研究中,哈佛大学的研究人员分析了50个大脑,其中一些来自没有阿尔茨海默病但有β-淀粉样蛋白斑块的人。他们发现,弹性大脑和患病大脑之间的一个关键区别是前者被激活的小胶质细胞少得多。
承认病原体假说有其优点,就意味着承认阿尔茨海默病研究领域长期以来一直是错误的。
如果淀粉样蛋白级联假说是正确的,那么从阿尔茨海默病患者的大脑中去除淀粉样蛋白斑块将会改善病症,或者至少不会使病症恶化。但事实并非如此,在2002年至2012年的十年间,在阿尔茨海默病临床试验中测试的145种降低β-淀粉样蛋白的药物中,尽管一些药物确实成功降低了β-淀粉样蛋白水平,但没有一种延缓疾病的进展。香港科技大学的分子神经科学家卡尔·赫鲁普(Karl Herrup)在2015年发表于《自然-神经科学》(Nature Neuroscience)的评论中写道:“现在是时候放弃淀粉样蛋白级联假说,寻找更合理的解释了。然而,该领域并没有拒绝这一假设,而是从本质上重新定义了这种疾病。导致阿尔茨海默病的研究陷入死循环。”
为什么研究人员以缺乏证据为由拒绝了病原体假说,却又支持缺乏数据支持的蛋白级联假说?在回应一篇米库洛丝的早期论文时,一群阿尔茨海默病研究人员解释称:“(他们)仍然谨慎对待甚至怀疑这样一种想法,即包括我们自己在内的许多人可能忽视能够科学治疗阿尔茨海默病的一种病因。”换句话说:承认病原体假说有其优点,就意味着承认阿尔茨海默病研究领域长期以来一直是错误的。
接受病原体假说可能还有更深的心理障碍。科学家们屡次难以接受微生物可以引起常见疾病的说法。胃溃疡就是一个特别著名的例子:尽管内科医生巴里·马歇尔(Barry Marshall)和病理学家罗宾·沃伦(Robin Warren)在20世纪80年代从澳大利亚的溃疡患者的肠道中分离出了幽门螺杆菌,并且抗生素在40年代末也成功地用于治疗溃疡,但主流科学家仍然拒绝相信它们可能具有传染性。最终马歇尔说服了全世界,他自己喝了一种细菌的混合物,这种混合物使他患上了胃炎,即溃疡的前兆,然后他用抗生素治愈了胃炎。同样,大概半个世纪后科学机构才相信,风湿热由链球菌引起,而在细菌感染和疾病发作之间有一段令人困惑的潜伏期。
考虑到导致阿尔茨海默病的神经退行性过程可能会持续数年,甚至数十年,它还涉及其余因素,所以这种观点难以被接受并不令人惊讶。霍尼格解释说:“我们倾向于对各行各业的复杂问题给出简单的回答,而在解决神经退行性疾病这一令人费解的谜团时,可能也是如此。追踪从感染到像阿尔茨海默病这样复杂疾病的路径,需要对各种研究声明有足够耐心,以及理解环境因素包括感染如何导致不同的结果。”
具有讽刺意味的是,一些科学家拒绝接受病原体假说,恰恰是因为他们过于简化这一假设。他们说,如果年龄或基因也是致病风险,感染就不可能是致病风险,换句话说,HSV-1分布太过广泛,所以认为它无致病风险。这些稻草人论证真正揭示的是,许多科学家没有花时间去理解这个病原体假说的细微差别和复杂性。
····
然而,撇开历史和偏见不谈,病原体假说肯定会引发更多问题,而不是提供答案。这一领域需要更多的研究(严格的研究),才能确定感染是否与阿尔茨海默病有因果关系。
当原因过多时,秉持科学的态度也很难。比如,研究人员只能在疾病确证后,才可以研究散发性阿尔茨海默病患者的大脑(无法提前知晓是否会患此病),这意味着他们无法观察到该病的初期病症。非营利组织阿尔茨海默病协会(Alzheimer Association)的科学和医疗业务高级主管希瑟·斯奈德(Heather Snyder)说:“你知道最终会发生什么,但由于大脑的复杂性,能否及时治疗才是真正的挑战。”
找到潜伏在中枢神经系统中的微生物也很困难。一个广泛被引用的局限是,对于那些将单纯疱疹病毒-1型与阿尔茨海默病联系起来的研究来说,还没有人能在已故阿尔茨海默病患者的大脑中分离出整株单纯疱疹病毒-1型;科学家只能检测到这种病毒的基因,理论上这种病毒可能来自已死亡病毒或其碎片。但是这种病毒又只是偶尔地重新激活,所以病毒只能在短时间内在大脑中循环。即使病毒确实存在,它们仍然很难被分离。当芬兰的研究人员试图从单纯疱疹病毒性脑炎患者的脊髓液中分离这种病毒时,他们能够成功的机会不足2%。霍尼格解释说:“如果致病因子的含量太低,或者它之前还未被其他研究发现,即使是脑组织活检也可能难以找出该因子。这也许是因为样本是在错误的脑区采集的,或者是在感染后期才采集的。”
大型制药公司继续投入研究资金用于抗β-淀粉样蛋白治疗,但在过去15年中,没有一项临床试验得到显著改善。
用抗微生物药物预防或治疗感染可以降低阿尔茨海默病的风险,是证明病原体假说正确的一种方法。当然,这需要在适当的时间给予适当的药物,这就使情况复杂化了。尽管如此,伊扎克本人多年来一直主张进行抗病毒药物的临床试验,虽然这些试验还没有具体实行。她说:“目前还没有任何反对进行试验的科学论据,所以只是资金问题。”
事实上,在试图研究病原体假说的研究人员中,资金一直是主要问题。罗宾逊说:“绝大部分资金继续用于与淀粉样蛋白级联假说相关的研究和试验。这种主导地位意味着,很少会有资源支持其他假设的研究。坦率地说,我感到惊讶的是,大型制药公司继续投入数亿美元用于抗β-淀粉样蛋白治疗,尽管在过去15年中没有一项临床试验得到显著改善。虽然阿尔茨海默病协会最近一直在扩大其关注范围——例如,自2011年以来,它资助了53个项目来调查阿尔茨海默病中的炎症——但在此期间,它只资助了一个与感染相关的项目。”
研究人员需要几十年的仔细研究才能解开连接感染、基因和阿尔茨海默病免疫力的复杂网络,前提是他们要获得足够的资金。尽管如此,莫尔说,他感觉到研究界正在慢慢地接受这种观点。他和他的同事们最近从马萨诸塞州的治愈阿尔茨海默病基金会(Cure Alzheimer’s Fund)获得了一些相关项目的资金,其中包括一个大脑微生物群项目。他们将对死后大脑中的基因进行测序,以确定隐藏在那里的微生物类型。2016年在韩国举行的一次神经退化会议上,认为感染可能与阿尔茨海默病有关的与会者被要求举手,大多数人都举了手。莫尔说:“要是十年前,大概就只有四个人挤在一个角落里,不跟任何人说话。我感觉验证这个观点的时机已经来临了。”
翻译:子铭
校对:雷胜
审校/编辑:EON
原文:https://aeon.co/essays/how-microbial-infections-might-cause-alzheimers-disease
现居纽约的科学作家,拥有纽约大学科学、卫生和环境报道硕士学位和分子生物学背景,在《Slate》上撰写专栏,《Scientific American》的特约编辑。