导语 / Introduction
日常生活,我们无时无刻不在感知酸甜苦辣、寒热温凉。但这些习以为常的温度感受与刺激反应,是如何在神经系统中转化为电脉冲的呢?
美国生理学家David Julius和美国分子生物学家Ardem Patapoutian因这方面的贡献荣获2021年诺贝尔生理学或医学奖。其中David Julius以辣椒素为始识别了热感受器,踏入了以往神经科学缺少的环节。
早晨上班,楼下便利店买一杯豆浆,两个香辣粉丝包,豆浆好烫,包子好辣,来不及吹凉。匆匆下肚,奔向地铁站的方向。车上人太多,空调有点冷,没站稳的姑娘,高跟鞋踩上脚趾,疼得龇牙咧嘴……
如此,一个被我们称为“我”的小人物,通过烫、辣、凉、冷、疼感受着此刻的世界。很难想象,这些感受能力消失了会是什么样。但我们确实因为这些感受的异常而不时苦恼:抓心挠肝般磨人的疼痛,越抓越剧烈的持续瘙痒,异常的冷和热,甚至还有癌症痛和神经痛。
人类一直试图探究意识的源起,也一直试图掌控我们的躯体。随着解剖学的进步,我们知道了神经元在感受传导中的神奇作用。但每时每刻感受着这个世界的神经元,如何区分酸甜苦辣咸、寒热温凉?决定神经元功能差异的,又会是神经细胞中的什么呢?
在很长一段时间内,科学家们猜测,神经细胞对不同刺激的不同响应,很可能依赖于细胞膜上的离子通道受体[1],[2]。离子通道受体,就如同房屋上的门窗,它的开放与关闭影响着细胞内外离子的进出,而对阴阳离子不同的选择性,又会影响细胞膜电位的变化。正常的细胞膜维持着外正内负的电位差,如果大量阳离子流入或者阴离子流出,都将导致细胞膜的去极化(静息电位向膜内负值减小的方向变化),达到一定水平,还将诱发动作电位(又称神经冲动),其可在神经细胞间不衰减地传导,如同电流在无阻抗电线中的传导一般,最终可到达大脑皮层,产生不同的感受。
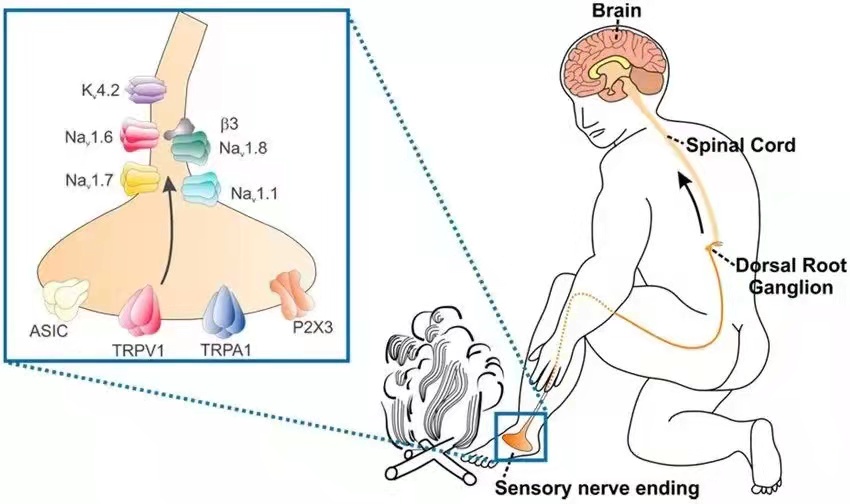
猜想变现实是极大的挑战,尤其是在我们还难以想象蛋白质如何对应对寒热温凉等物理化学刺激时,而实现这一伟大突破的是美国生理学家大卫·朱利叶斯(David Julius)。
上世纪九十年代,擅长受体克隆的朱利叶斯,开始对躯体感受与疼痛的分子机制产生兴趣。以辣椒为切入点,在经历重重困难后,他最终于1997年成功克隆出辣椒素特异性受体——香草素受体1型(TRPV1),并意外发现该受体可以被43℃以上的物理高温激活[3]。这一伟大的发现,首次呈现了离子通道受体在物理化学刺激间的信号转导作用,即辣椒素等天然化学物质刺激与温度等物理刺激,可通过细胞膜上TRPV1通道统一转化为电信号,从分子层面为我们展现了躯体感受认知的最基础的来源,更新了我们对躯体感受的认知。
此后的二十多年,朱利叶斯以TRPV1为起点,又相继发现了多种与躯体感受相关的TRP家族的通道蛋白。与此同时,他与同事程亦凡的实验室合作,解析了包括TRPV1在内的多种TRP蛋白的三维结构,并综合运用基因敲除等生理手段,试图回答这些神奇蛋白的结构与功能关系,为靶向药物开发提供理论基础。
如此开创性与系统性的研究工作,也使他陆续获得2020年度的生命科学突破奖与科维理神经科学奖(Kavli Prize)。
在2020年揭晓的科维理神经科学奖中,评审委员会主席克里斯汀·沃尔霍夫德(Kristine B. Walhovd)表示:“朱利叶斯和阿德姆·帕塔博蒂安(Ardem Patapoutian)的独立发现正在彻底改变我们对于感觉探测的认知,并将对解决全球健康和疾病问题产生深远影响。”
而在今天,他们也因发现温度与触觉感受器,荣获诺贝尔生理学或医学奖。
2021诺贝尔生理学或医学奖
大卫·朱利叶斯 David Julius

美国的神经生物学家,1977年在麻省理工学院获得了生命科学学士学位,1984年在加州大学伯克利分校获得生物化学博士学位。此后,他加入了哥伦比亚大学,因着对神经药理学的兴趣,他克隆了血清素的几种受体,并获得了1990年NSF总统青年研究者奖。自1990年以来,他在加州大学旧金山分校任职,并发现了一个对温度和化学刺激敏感的离子通道家族,为触摸和疼痛感提供了分子基础。目前,他正担任莫里斯·赫兹斯坦(Morris Herzstein)分子生物学和医学主席、生理学教授和主席,并继续这项研究。
他于2004年当选为美国国家科学院院士,2005年当选为美国艺术与科学学院院士,并因在辣椒素和温度方面的TRPV1受体研究工作,成为匈牙利科学院的名誉会员。最近他获得的其他奖项包括2017年加拿大盖尔德纳国际奖、2019年罗森斯蒂尔基础医学奖和2020年生命科学突破奖。
阿德姆·帕塔博蒂安 Ardem Patapoutian

分子生物学家,专门研究神经系统中的感觉信号。在1986年移居并成为美国公民之前,他就读于贝鲁特美国大学。于1990年获得了加州大学洛杉矶分校的科学学士学位,随后在位于帕萨迪纳的加州理工学院获得了发育生物学博士学位。1996年,他与路易斯·里卡特(Louis Reichardt)一起去了加州大学旧金山分校进行神经生长因子的博士后研究。
他于2000年加入斯克里普斯研究所,现任神经科学教授。他领导了涉及感知温度和触觉,以及本体感觉和血压的调节的离子通道和受体的识别工作。他最近获得的荣誉包括2017年哥伦比亚大学的阿尔登·斯宾塞奖(与David Ginty分享)和2019年罗森斯蒂尔基础医学研究杰出工作奖(与David Julius分享)。他于2014年被任命为霍华德·休斯医学研究所的研究员,并于2017年当选为美国国家科学院院士,于2020年当选为美国艺术与科学院院士。
辣椒的痛与镇痛
在刚发现辣椒素受体TRPV1时,人们对能将化学和物理信号转变为电信号的蛋白受体感到相当兴奋。但与此同时,人们又惊讶地发现辣不是一种味觉,而是一种痛觉。
究其原因,TRPV1受体特异性表达于伤害性感受神经元(特异性识别伤害性刺激的传入神经元),且在身体多种组织器官内广泛分布。当有辣椒或者高温刺激时,TRPV1受体立即被激活,产生电信号,信号沿伤害性传入神经系统上传至大脑。又因为大脑对伤害性传入神经信号的解读统一为“疼痛”的刺激感,所以辣觉被科学地定义为痛觉[3](当然,辣痛与普通疼痛存在区别,源于它的热感受属性)。这就不难解释,为什么除了嘴巴,我们的眼睛和皮肤也会有辣痛感。
如何科学解辣?
- 破坏辣椒素与TRPV1受体间的结合,如饮用油脂高的食物或饮料(牛奶、豆奶、奶油冰激凌等),从而溶解结合于受体上的辣椒素。
- 干扰大脑对辣的感受过程,例如蔗糖和香草素就有不错的解辣效果。香草素解辣的原因比较复杂,而蔗糖解辣一方面是因为甜与辣的刺激作用于口腔中不同的受体细胞,受体细胞之间的相互作用干扰大脑意识的产生,另一方面,大脑在接受甜刺激后会释放镇痛物质,进而缓解辣的痛感。
- 还有一个有趣的研究发现,捏紧鼻孔能抑制50%的辣感受,原因是鼻孔关闭,舌头表面温度会随之降低,而温度的降低又会减少TRPV1激活的可能。(下次辣到崩溃,也许你可以第一时间试试捏紧鼻子[4]?)
除了餐桌上的调味剂,人们还一直将辣椒当作镇痛剂。但直到TRPV1发现之后,辣椒的镇痛奥秘才浮出水面:TRPV1的离子通道性质在被持续激活时,阳离子将不断地涌入细胞,而过多的钙离子可产生细胞毒性,细胞出于自身保护便会反馈性地关闭TRPV1通道,并使伤害性感受神经元对辣椒素甚至其他伤害性刺激脱敏,减少痛觉信号的产生,由此抑制疼痛感受。
抓住TRPV1受体与镇痛的关系后,科学家们便将其视作治疗多种慢性疼痛的新的重要药物靶标。大型制药公司纷纷入局,通过模拟和提升辣椒素对于TRPV1通道的激活作用,或者直接抑制通道功能,来阻断大脑对疼痛的感知,寄希望于研发出新的高效的止痛药,以补充已有药物在治疗上的局限与强风险(阿片类药物存在成瘾性问题,一些抗炎止痛药具有肝脏和心血管损伤风险)。目前,已有十几种相关药物进行到各阶段的临床试验,比如生物制药公司Centrexion Therapeutics推出的超纯合成辣椒素(反式异构体)制剂CNTX-4975[5]。该制剂通过一个特殊注射装置导向骨关节注射,治疗膝关节中度至重度疼痛,目前已进入三期临床试验。
“火辣”开启温度觉探索的大门
让我们感到痛的同时,辣椒又为什么会让我们觉得热呢?
如前所述,TRPV1受体在被辣椒素激活时,还可被43℃以上的物理高温激活。在TRPV1之后,大卫·朱利叶斯和其他科学家团队又相继发现,多种与TRPV1相类似的离子通道蛋白(共属于TRP蛋白家族)与温度感受相关。例如,同样获得科维理神经科学奖的阿德姆·帕塔博蒂安(Ardem Patapoutian)的团队,在2002年通过薄荷醇分子(薄荷的主要成分),确认了一类薄荷醇敏感离子通道TRPM8,该通道能被8℃~28℃的无害低温激活[6]。2003年,该团队又发现了可被芥末激活的冷觉感受通道——TRPA1,它能被超低温(<17℃)激活[7]。
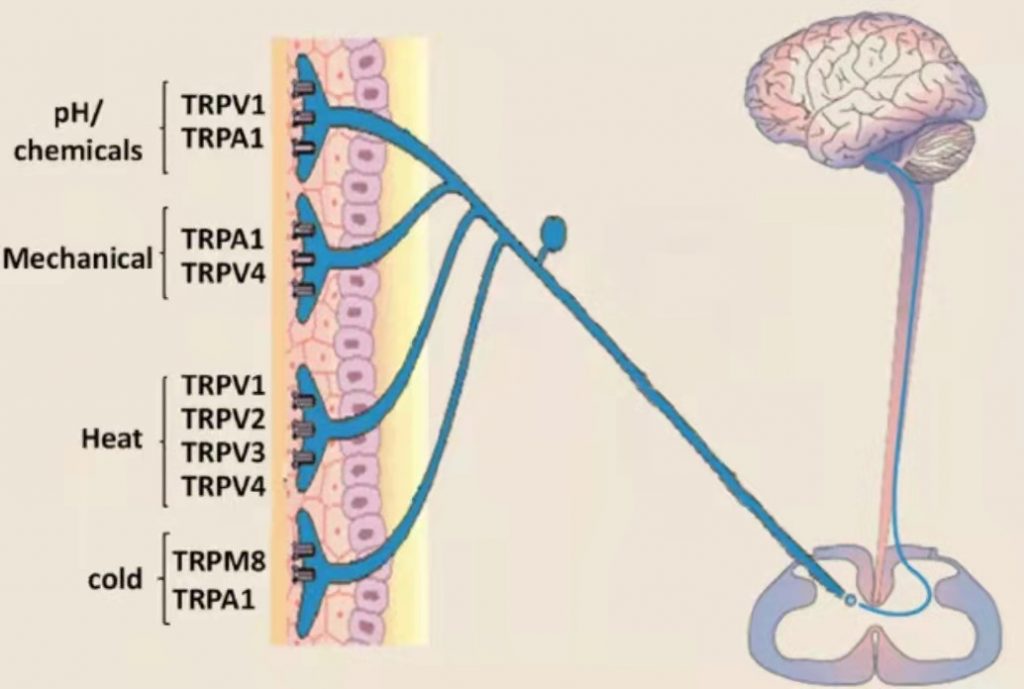
目前,我们已经可以从分子层面基本推断寒热温凉感受的来源:初级感觉神经元表达多种与温度感受相关的TRP通道亚型,例如,感受伤害性热的TRPV1(≥42℃),TRPV2 (≥52℃)[8],TRPM3(≥40℃)[9];感受非伤害性热的TRPV3 (≥31℃)[10],TRPV4(≥ 25℃)[11], TRPM2(≥35℃)[12],TRPM4/TRPM5(15-25℃)[13];感受非伤害性冷的TRPM8 (≤28℃);感受伤害性冷的TRPA1(≤17℃)以及感受温度降低的TRPC5(25-37°C)[14]。当机体处于不同的温度环境时,特异性的温度敏感型离子通道将被激活产生电信号,经神经系统传输至大脑,产生特定的温度感受[15]。
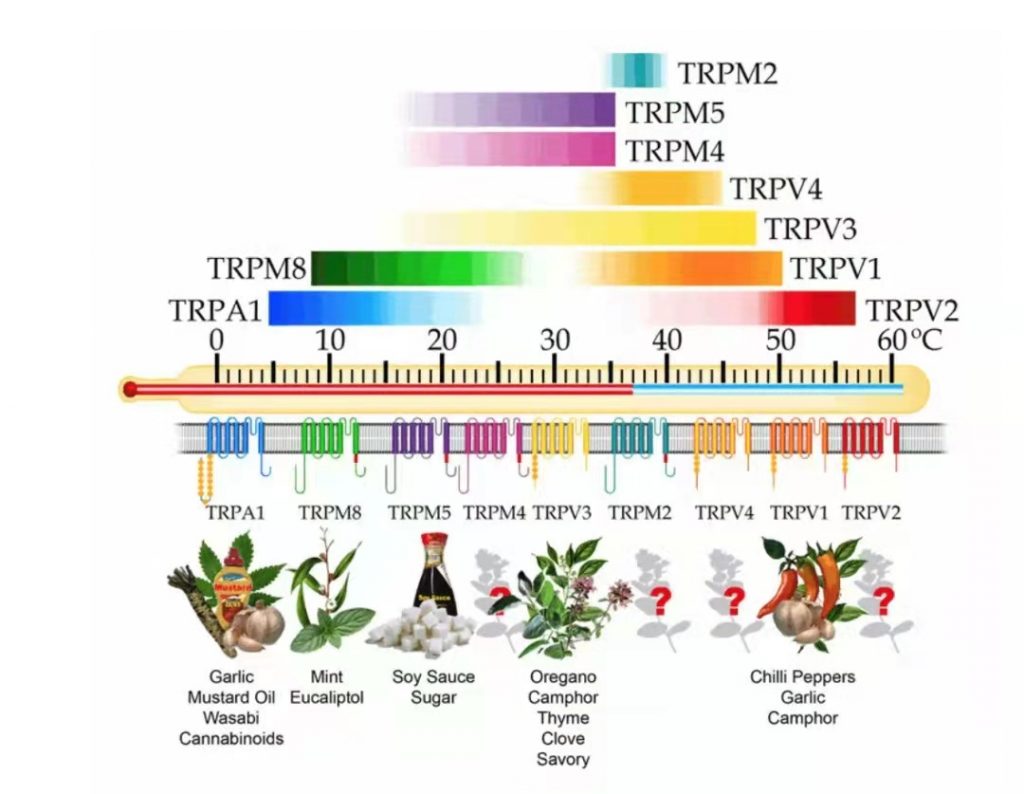
有趣的是,感受寒热温凉的蛋白受体竟不是专司其职,反而“一心多用”,以至于造就了辣椒火热、薄荷清凉的神奇体验。那么问题来了,我们吃辣椒时感受到的热,真的与物理温度升高有关吗?换言之,我们所说的热性/易上火类物质“热”在哪儿?
可以肯定的是,食用辣椒类物质的热并非物理温度改变的结果,而是感受上的结果。大家可能都有过这样的感受:被辣到后对热的感受更敏感了。这是因为可同时被辣椒素与物理高温(≥42℃)激活的TRPV1通道,在被辣椒素激活后,对温度感受的阈值降低,即不到42℃的体温也能诱发伤害性“热”感受;同时,辣椒素与温度对TRPV1受体的双激活,也大大增强了表达有该受体的感觉神经元的兴奋性。因此我们的感受被“异常”放大,即使一口40℃的辣汤就有“喷火”感。
如果辣椒的热感是大脑的“异常感知”,那我们担心吃辣加剧口腔溃疡的所谓“上火”又作何解释?这取决于TRPV1受体在信号传导中的性质。
由于TRPV1受体是在神经与非神经组织中都有表达的非选择性阳离子通道,它的激活会介导大量钙离子内流,产生电信号的同时,在非神经组织中,胞内增高的钙离子浓度,还将介导多种神经肽的释放,如P物质(SP)和降钙素基因相关肽(CGRP)。SP可以引发血管舒张和血管通透性增加,导致水肿形成,还可以刺激肥大细胞释放组胺等炎症介质,诱导白细胞释放蛋白酶和活性氧(ROS)。CGRP能放松动脉,也能调节皮肤血流量的增加),引起神经源性炎症[16]。
所以“上火”与火无关,而是机体出于“自身防御”诱发的炎症反应。虽然我们习惯视疼痛与炎症为疾病,但疼痛与炎症存在的初衷是保护机体远离伤害,与炎症相关联的是免疫,红肿处的炎症就如一面标着“SOS”的小红旗,大声提醒免疫系统:“嘿,伙计,此处有破坏份子”。
除辣椒素外,乙醇、类胰蛋白酶、树脂毒素、大蒜素、姜油、芥子油等也都能引发神经源性炎症,它们正好源于我们常说的几种“上火”食物:酒精、菠萝、蒜头、生姜……而更有趣的是,TRP家族中很多蛋白亚型,也正是这些“上火”物质的受体(参见图二),比如冷觉受体TRPA1又称为“芥末受体”,可被芥子油、大蒜素甚至吸烟时的烟雾激活。最近还有研究把TRPA1称为“咳嗽的开关”:研究人员利用纸烟烟雾中含有的丙烯醛等物质进行试验,发现无论老鼠还是志愿者,吸入这些物质后都会咳嗽。吸入量越大,咳嗽越厉害。但如果用药物抑制体内的TRPA1受体,他们的咳嗽程度就会明显减轻。目前这一发现已用于研发治疗慢性咳嗽的药物[17]。
TRP家族与光感受
从疼痛到温度觉的解密,TRP家族快速地填充我们对感受的认知。让我们将时间轴拉回20世纪60年代,当时的科学家们运用多种诱变方法处理果蝇,希望能在不同的诱变型中有新的科学发现,而TRP就是其中之一。
1969年,科曾斯(Cosens)和曼宁(Manning)发现一种有着异常趋光性和视网膜电位的突变果蝇品系[18],猜想该突变基因可能表达了一种光受体。1975年,随着电生理技术的进步,威廉·帕克(William Pak)实验室终于获得该突变体与野生型果蝇在单个光感受细胞上的电位差异,以及突变体对光反应是瞬时的电位变化特征,于是首次将该突变体命名为瞬时受体电位(TRP)[19]。自此,TRP通道在光感受上的作用成了新的科学问题。
2000年以后,随着TRPV1和TRPA1受体研究的增多,最新发现TRPV1和TRPA1受体对紫外线有响应[20]。紫外线和蓝光可产生单态氧,而单态氧又起到TRPA1和TRPV1激动剂的作用,增强其对光敏感性[21]。这一发现对于那些暴露于阳光下,有着异常疼痛与灼烧感的皮肤卟啉症患者,以及在接受光动力疗法治疗的癌症患者极其重要[20],[22]。
结语
至此,我们已从辣椒素受体的发现开始,逐步了解了离子通道受体在痛觉、温度觉以及光感受中的神奇作用,见识到了TRP这个宝藏家族的多元技能。芥末葱姜蒜、寒热温凉痛,电压机械力,无不与其相关。
当然,TRP蛋白家族在生命活动中的功能并不局限于此,既不能认为所有的TRP通道都是感觉受体,也不能认为所有的感觉受体都是TRP通道[23]。在TRP家族之外,帕塔博蒂安发现的Piezo蛋白家族与躯体压力感受间的关联,也是一个极其宏大的科学问题,可从触觉、听觉、本体感受等维度解释我们对这个世界的机械感知[24]。而这,就是另一篇故事了。
参考文献
[1]Krishtal OA, Pidoplichko VI. A receptor for protons in the membrane of sensory neurons may participate in nociception. Neuroscience. 1981;6(12):2599-2601. doi:https://doi.org/10.1016/0306-4522(81)90105-6
[2] Waxman SG, Zamponi GW. Regulating excitability of peripheral afferents: emerging ion channel targets. Nat Neurosci. 2014;17(2):153-163. doi:10.1038/nn.3602
[3] Caterina MJ, Schumacher MA, Tominaga M, Rosen TA, Levine JD, Julius D. The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature. 1997;389(6653):816-824. doi:10.1038/39807
[4] Smutzer G, Jacob JC, Tran JT, et al. Detection and modulation of capsaicin perception in the human oral cavity. Physiol Behav. 2018;194:120-131. doi:https://doi.org/10.1016/j.physbeh.2018.05.004
[5] Stevens RM, Ervin J, Nezzer J, et al. Randomized, Double-Blind, Placebo-Controlled Trial of Intraarticular Trans-Capsaicin for Pain Associated With Osteoarthritis of the Knee. Arthritis Rheumatol (Hoboken, NJ). 2019;71(9):1524-1533. doi:10.1002/art.40894
[6] Peier AM, Moqrich A, Hergarden AC, et al. A TRP Channel that Senses Cold Stimuli and Menthol. Cell. 2002;108(5):705-715. doi:https://doi.org/10.1016/S0092-8674(02)00652-9
[7] Story GM, Peier AM, Reeve AJ, et al. ANKTM1, a TRP-like Channel Expressed in Nociceptive Neurons, Is Activated by Cold Temperatures. Cell. 2003;112(6):819-829. doi:https://doi.org/10.1016/S0092-8674(03)00158-2
[8] Caterina MJ, Rosen TA, Tominaga M, Brake AJ, Julius D. A capsaicin-receptor homologue with a high threshold for noxious heat. Nature. 1999;398(6726):436-441. doi:10.1038/18906
[9] Vriens J, Owsianik G, Hofmann T, et al. TRPM3 Is a Nociceptor Channel Involved in the Detection of Noxious Heat. Neuron. 2011;70(3):482-494. doi:https://doi.org/10.1016/j.neuron.2011.02.051
[10] Singh AK, McGoldrick LL, Demirkhanyan L, Leslie M, Zakharian E, Sobolevsky AI. Structural basis of temperature sensation by the TRP channel TRPV3. Nat Struct Mol Biol. 2019;26(11):994-998. doi:10.1038/s41594-019-0318-7
[11] Güler AD, Lee H, Iida T, Shimizu I, Tominaga M, Caterina M. Heat-Evoked Activation of the Ion Channel, TRPV4. J Neurosci. 2002;22(15):6408 LP – 6414. doi:10.1523/JNEUROSCI.22-15-06408.2002
[12] Tan C-H, McNaughton PA. TRPM2 and warmth sensation. Pflügers Arch – Eur J Physiol. 2018;470(5):787-798. doi:10.1007/s00424-018-2139-7
[13] Talavera K, Yasumatsu K, Voets T, et al. Heat activation of TRPM5 underlies thermal sensitivity of sweet taste. Nature. 2005;438(7070):1022-1025. doi:10.1038/nature04248
[14] Zimmermann K, Lennerz JK, Hein A, et al. Transient receptor potential cation channel, subfamily C, member 5 (TRPC5) is a cold-transducer in the peripheral nervous system. Proc Natl Acad Sci. 2011;108(44):18114 LP – 18119. doi:10.1073/pnas.1115387108
[15] Tominaga M. The Role of TRP Channels in Thermosensation. In: ; 2006:271-286. doi:10.1201/9781420005844.ch20
[16] Bujak JK, Kosmala D, Szopa IM, Majchrzak K, Bednarczyk P. Inflammation, Cancer and Immunity—Implication of TRPV1 Channel. Front Oncol. 2019;9:1087. doi:10.3389/fonc.2019.01087
[17] Morice AH. TRPA1 receptors in chronic cough. Pulm Pharmacol Ther. 2017;47:42-44. doi:https://doi.org/10.1016/j.pupt.2017.05.004
[18] COSENS DJ, MANNING A. Abnormal Electroretinogram from a Drosophila Mutant. Nature. 1969;224(5216):285-287. doi:10.1038/224285a0
[19] MINKE B, WU C-F, PAK WL. Induction of photoreceptor voltage noise in the dark in Drosophila mutant. Nature. 1975;258(5530):84-87. doi:10.1038/258084a0
[20] Babes A, Sauer SK, Moparthi L, et al. Photosensitization in Porphyrias and Photodynamic Therapy Involves TRPA1 and TRPV1. J Neurosci. 2016;36(19):5264 LP – 5278. doi:10.1523/JNEUROSCI.4268-15.2016
[21] Hill K, Schaefer M. Ultraviolet light and photosensitising agents activate TRPA1 via generation of oxidative stress. Cell Calcium. 2009;45(2):155-164. doi:https://doi.org/10.1016/j.ceca.2008.08.001
[22] Cun-Jin S, Jian-Hao X, Xu L, et al. X-ray induces mechanical and heat allodynia in mouse via TRPA1 and TRPV1 activation. Mol Pain. 2019;15:1744806919849201. doi:10.1177/1744806919849201
[23] Rohacs T. Phosphoinositide signaling in somatosensory neurons. Adv Biol Regul. 2016;61:2-16. doi:https://doi.org/10.1016/j.jbior.2015.11.012
[24] Murthy SE, Dubin AE, Patapoutian A. Piezos thrive under pressure: Mechanically activated ion channels in health and disease. Nat Rev Mol Cell Biol. 2017;18(12):771-783. doi:10.1038/nrm.2017.92
作者:一一 | 编辑:EON | 插画:纪善生



上海交通大学医学院基础医学博士在读,目前主要研究离子通道结构与功能。对精神疾病的关注源于抑郁症经历,可以说,抑郁症在一定程度上重塑了我的生活,从理解问题的视角,对自我的认识,以及到科研工作方向的选择等方方面面。现在,在神经科学方面,我最大的心愿是能尽自己所能去发现抑郁症及其他精神疾病发生的生理基础,或者说情绪如何实现在生理层面对我们机体的影响,当然,生理与心理的交互这是一个巨大的议题,我愿成为这个议题发展路上的一块砖。
















评论